SBRT chorych z przerzutami do kości w lokalizacji poza kręgosłupem – przegląd systematyczny, metaanaliza i wytyczne ISRS
W zielonym żurnalu opublikowano wytyczne International Stereotactic Radiosurgery Society dotyczące stosowania SBRT u chorych
z przerzutami do kości poza kręgosłupem (non-spine bone metastases, NSBM).
Autorzy przeanalizowali 18 badań, w których łącznie przeprowadzono SBRT u 1499 pacjentów z 1590 NSBM. Najczęstsza lokalizacja zmian: miednica, żebra, kończyny.
Kontrola miejscowa (LC) i przeżycie całkowite (OS) po 1 i 2 latach wyniosły odpowiednio: 95% i 94% (LC) oraz 84% i 81% (OS).
Pozytywny wpływ na OS: rozpoznanie raka gruczołu krokowego, negatywny: rozpoznanie raka płuc, lokalizacja w obrębie miednicy lub żeber. Zastosowana dawka (BED10) nie wpływała na 1-y OS.
Najczęściej stosowane schematy – 18-24Gy/1fx, 27-30Gy/3fx, 30-35/5fx.
NSBM SBRT jest dobrze tolerowanym leczeniem z niskim odsetkiem AE. Najczęstsze powikłania w st. G1/2 – zmęczenie, ból, nudności
i wymioty. Najczęstszym późnym AE jest złamanie kości (<17%).
Zalecenia ISRS
- Planowanie SBRT
- CT do planowania leczenia ze skanami maksymalnie co 3mm. W przypadku małych przerzutów lub lokalizacji blisko krytycznych struktur anatomicznych – skany co 1mm (jakość dowodów 5).
- Zaleca się wykonanie bad. MR do planowania SBRT (do 3 tyg. przed początkiem leczenia) i jego fuzję z CT; przydatne w przypadku nacieku tkanek miękkich lub słabej widoczności zmiany w CT (jakość dowodów 4).
- Można dołączyć bad. PET/CT – rola pomocnicza w ustalaniu lokalizacji GTV (jakość dowodów 5).
- W przypadku przerzutów zlokalizowanych w żebrach i mostku (wyjątek: żebra tylno-przyśrodkowe oraz górna część mostka) rozważyć zastosowanie technik kontroli ruchomości, np. 4DCT, aktywna kontrola oddechu (jakość dowodów 5).
- Rozważyć zastosowanie maski termoplastycznej w przypadku zmian na poziomie Th4 i wyżej (jakość dowodów 5).
- Wyznaczenie GTV
- Wykorzystać fuzję CT do planowania SBRT i inne dostępne badania obrazowe (MRI, PET/CT); GTV wyznaczać w oknie kostnym
i miękkotkankowym (jakość dowodów 4)
- Wykorzystać fuzję CT do planowania SBRT i inne dostępne badania obrazowe (MRI, PET/CT); GTV wyznaczać w oknie kostnym
- Wyznaczenie CTV
- W przypadku wyznaczania GTV na podstawie MRI +/- PET/CT zaleca się dodanie do GTV marginesu 0–5 mm; GTV wyznaczony jedynie na CT – do GTV dodać 5-10mm marginesu obejmującego przylegającą tkankę kostną (jakość dowodów 5).
- W przypadku nacieku pozakostnego lub przerwania warstwy korowej kości rozważyć dodanie do GTV marginesu 5mm obejmującego tkanki poza kością. Zmiana ograniczona do kości bez przerwania warstwy korowej – CTV nie powinien wykraczać poza kość. Dostosować CTV do naturalnych barier anatomicznych, np. otrzewna, opłucna (jakość dowodów 5).
- Zalecany margines PTV - zazwyczaj 2-5mm (jakość dowodów 5).
- Schematy frakcjonowania
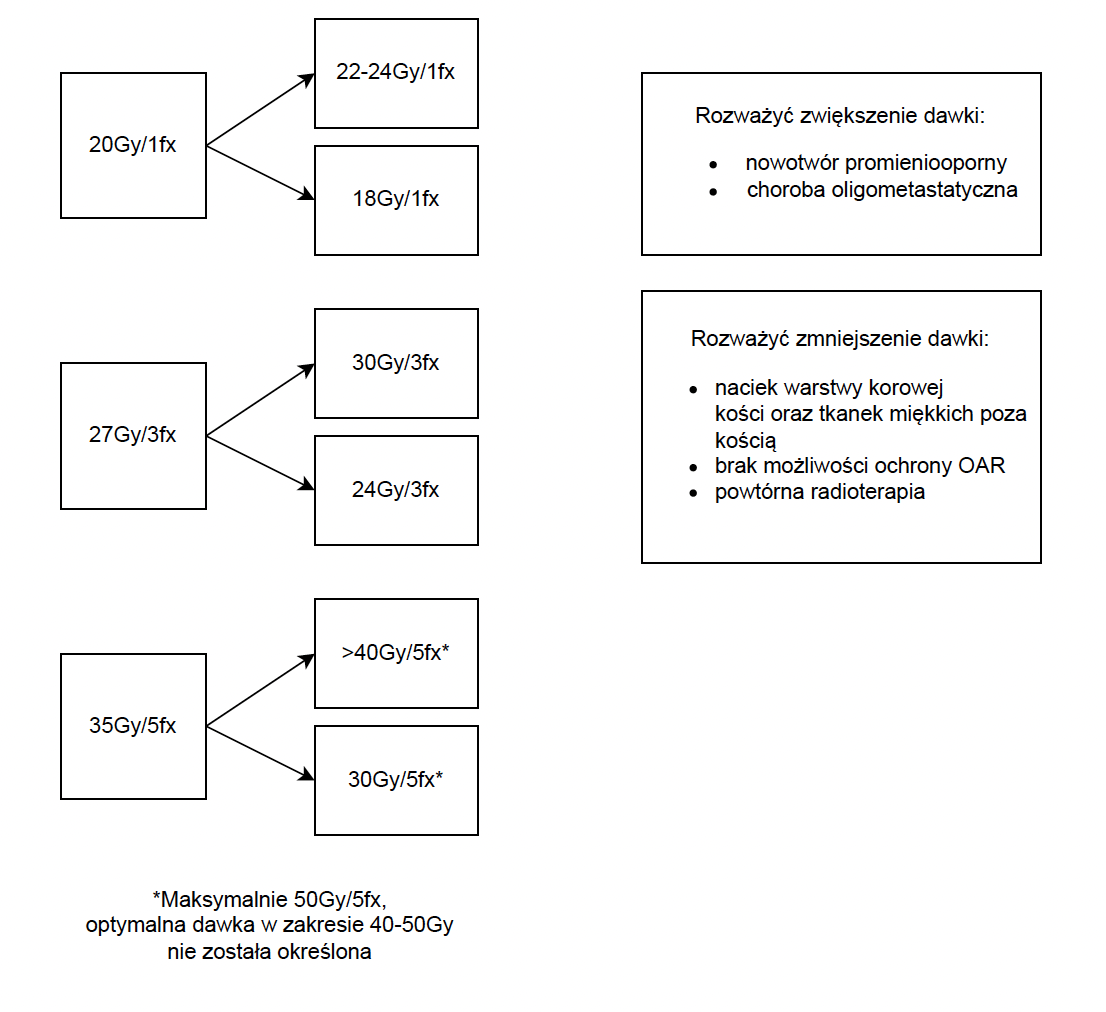
- Zalecane schematy SBRT: 18-24Gy/1fx, 27-30Gy/3fx, 30-35/5fx (jakość dowodów 5).
- Należy rozważyć deeskalację w przypadku powtórnej SBRT, braku możliwości ochrony OAR, nacieku warstwy korowej kości, nacieku pozakostnego (jakość dowodów 5).
- Eskalacja dawki jest zalecana w przypadku nowotworów opornych na promieniowanie, choroby oligometastatycznej z intencją wyleczenia (jakość dowodów 5).
- W przypadku zmian w kościach długich zaleca się stosowanie schematów frakcjonowanych, aby zmniejszyć ryzyko złamania.
Ostrożnie eskalować dawkę powyżej 27-30Gy/3fx lub 30-35Gy/5fx (jakość dowodów 5).
Zalecany przez ISRS algorytm wyboru schematu SBRT:
- SBRT zmian w obrębie obręczy barkowej, kości ramiennej, łokciowej i promieniowej
- Rozważyć odsunięcie leczonej kończyny od tułowia, aby zminimalizować dawkę w płucach i ścianie klatki piersiowej. Target w kości ramiennej, łokciowej lub promieniowej – rozważyć zastosowanie unieruchomienia, aby ograniczyć rotację np. VacLoc (jakość dowodów 5).
- Obojczyk lub łopatka – w celu ułatwienia lokalizacji targetu należy, jeśli to możliwe, rozważyć utrzymanie takiej samej pozycji ramion jak podczas badań diagnostycznych (jakość dowodów 5).
- SBRT zmian w obrębie klatki piersiowej
- Ruchomość oddechowa targetu powinna być oceniona za pomocą 4D-CT. Można zastosować bramkowanie oddechowe, abdominal compression lub aktywną kontrolę oddechu, z wyj. lokalizacji w proksymalnym odcinku żebra lub w górnej części mostka (jakość dowodów 5).
- Zaleca się stosowanie schematów frakcjonowanych w przypadku leczenia zmian w żebrach (jakość dowodów 5).
- W przypadku leczenia zmian w mostku należy uwzględnić dawkę w skórze (jakość dowodów 5).
- SBRT zmian w obrębie kończyny dolnej
- Panewka stawu biodrowego – stosować schematy frakcjonowane; jeśli PTV obejmuje przestrzeń stawową, zaleca się deeskalację dawki, np. 30Gy/5fx (jakość dowodów 5).
- Kość udowa, piszczelowa lub strzałkowa – w przypadku lokalizacji targetu poniżej poziomu kolana, rozważyć zastosowanie unieruchomienia, np. VacLoc (jakość dowodów 5).
Źródło: https://linkinghub.elsevier.com/retrieve/pii/S0167-8140(25)00012-X
AN/IZ